|
檢驗項目 |
HLA-B 5801(for Allopurinol) |
院內醫令碼 |
L1221301 |
|
中文名稱 |
HLA-B*5801基因檢測 (安樂普利諾) |
健保代碼 |
12213B |
|
適用檢體別 |
血液 |
支付點數 |
2343 |
|
建議採檢容器 |
檢驗操作方法 |
Real-time PCR |
|
|
檢體採集量 |
至少1mL |
||
|
送檢方式 |
人工傳送/氣送 |
生物參考區間/臨床決策值(單位) |
Non-detected |
|
收檢時間 |
24小時 |
||
|
報告時效 |
8天 |
採檢容器料號 |
M3110016 |
|
操作組別/分機 |
義大醫院 基因診斷組/5807 |
其他備註事項 |
|
|
檢驗操作時間 |
週二 |
||
|
採檢應注意事項 |
採檢後,請180度輕微搖晃4~5次,以利抗凝劑混合均勻。 |
||
|
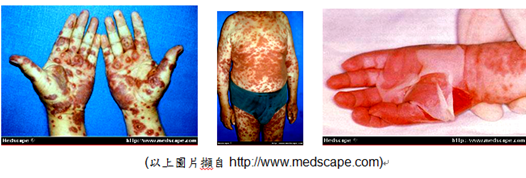
臨床意義與用途: HLA基因位在人類的第六條染色體的短臂上,主要分成兩大類,第一類主要有A、B、C三種,第二類有DP、DQ、DR;不同人類個體之間的HLA具有高度多型性(Highly polymorphism),各自的HLA型別是來自己的父母親,所以兄弟姐妹之間有接近四分之ㄧ的機會完全相同,若父親或母親有一位是HLA-B*5801的帶因者,則該夫妻的小孩也會有1/2的機會是HLA-B*5801的帶因者。 哪些人需要做HLA-B*5801基因檢測? HLA-B*5801基因被發現對於華人因使用Allopurinol(安樂普利諾)藥物而引起『高過敏反應/史蒂芬強森症候群/毒性表皮溶解(HSS/SJS/TEN,合稱嚴重皮膚藥物不良反應SCARs)』的風險是無HLA-B*5801基因患者的700倍以上。 Allopurinol通常是用於痛風症、痛風性關節炎、尿酸結石、癌症或經化學治療產生之高尿酸血症,台灣族群帶有HLA-B*5801基因的盛行率比歐洲族群及日本族群高,臨床醫師在使用此類藥物之前均建議先進行HLA-B*5801基因檢測,以加強病患之用藥安全。 史蒂芬強森症候群(Steven-Johnson Syndrome,SJS)/毒性表皮溶解(Toxic Epidermal Necrolysis, TEN) 史蒂芬強森症候群為一種常見的藥物嚴重過敏反應,是西元1920年由美國小兒科醫生史帝文生(Albert Stevens)和強生(Frank Johnson)發現,患者通常是吃了某類藥物約數天後,皮膚開始起疹子和水泡,消化道、呼吸道、眼睛及/或嘴巴的黏膜受損,嚴重甚至導致失明。臨床上,當皮膚剝落程度超過30%,稱做「毒性表皮溶解」(Toxic Epidermal Necrolysis, TEN),致死率高達30%。SJS/TEN真正發生的原因不明,通常與感染、藥品及抵抗力減退之狀態有關,其發生率不分年齡、種族、季節與性別。
基因檢測的侷限性 利用即時聚合酶連鎖反應方法來檢測HLA-B*5801基因的有無,其準確度雖達到99.5%以上,但仍有下列臨床診斷的侷限性:
健保適應症
註一、本檢驗試劑使用PHARM i-Gene PG5801 Detection Kit,以即時聚合酶連鎖反應定性檢測HLA-B*5801基因。根據原廠說明,此檢驗相對於基因定序方法之特異性與敏感度可達100%。可能造成偽陽性結果之非HLA-B*5801基因型別:HLA-B*5705、5804、5805、5809、5810、5811、5812、5813、5815、5817、5819、5821、5822、5823、5824、5828等共16型。 註二、本試驗偵測極限(detection limit)為10 ng/reaction,因此檢測檢體DNA濃度應維持於12.5-50 ng/µl方能維持檢驗品質,濃度不足時將於報告中備註。 |
|||
 義大醫學檢驗部
品質-服務-研究-教學-效率-卓越
義大醫學檢驗部
品質-服務-研究-教學-效率-卓越